按照《医疗器械生产许可证》申请要求,2022年5月18日郑州航空港区经济综合试验区市场监督管理局司处长一行莅临郑州耐视医药科技有限公司开展现场检查工作。
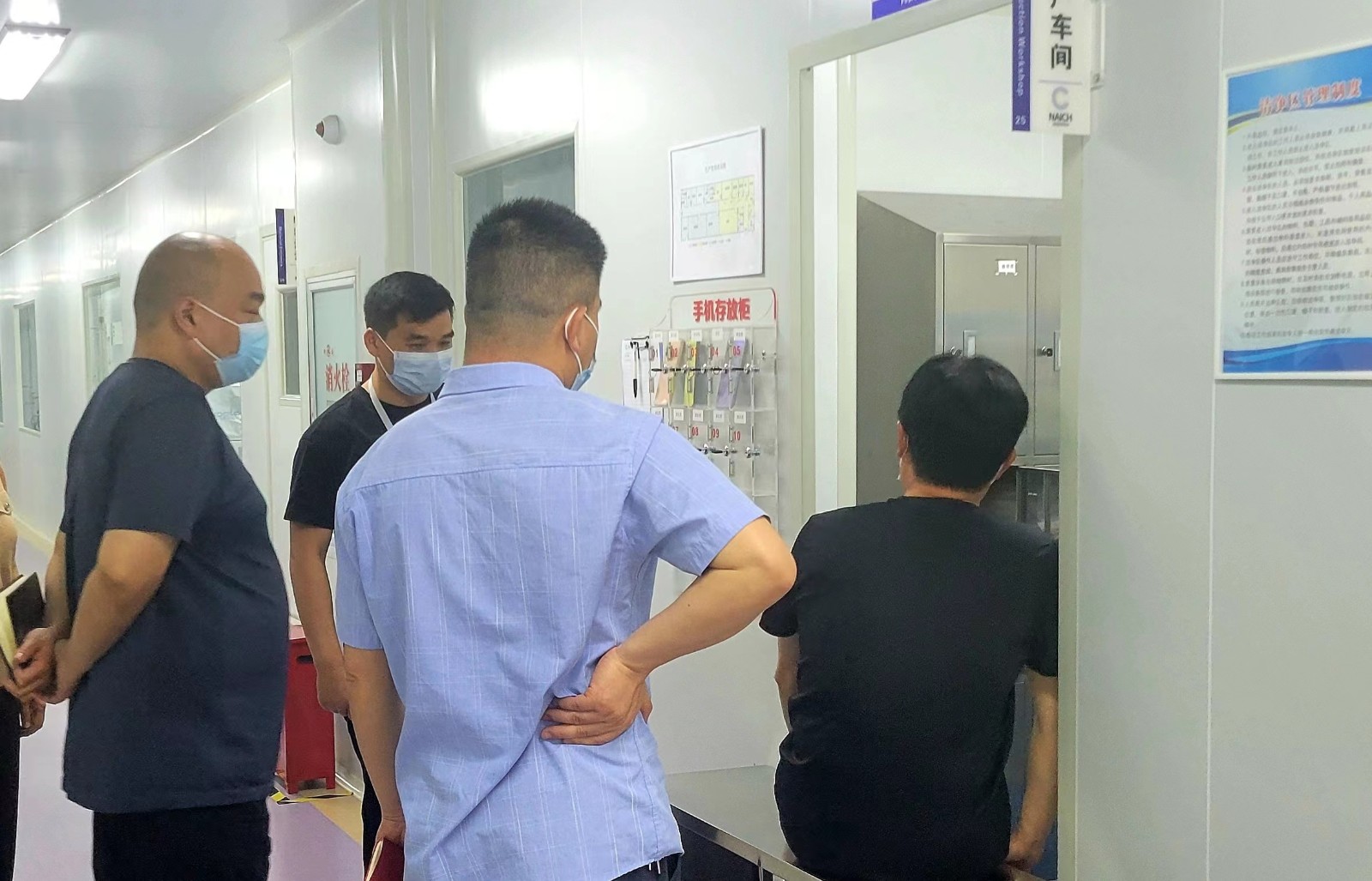
检查组正在做进入车间前准备工作
经过一天全面、严格、细致的检查,检查组认为郑州耐视医药科技有限公司各项管理制度完善、质量管理体系系统运行良好、机构与人员符合要求、经营场所与储备条件达标、具备人工晶状体植入系统的生产能力,符合医疗器械生产许可相关要求,顺利通过现场检查。
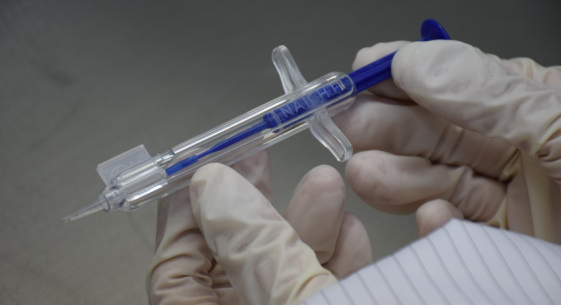
推注杆与推注主体组装
检查过程中,检查组认真听取了耐视医药厂区负责人关于企业总体情况的汇报,并抽查了产品设计图纸、产品说明书、 生产记录、人员档案 等资料。现场检查过程中检查组深入车间对环境、人员操作情况、以及相关记录等内容进行了详细检查。

生产工作台
此次《医疗器械生产许可证》注册申请的现场检查,不仅是对郑州耐视医药科技有限公司的一次大考,更是对公司经营理念、管理水平的一个高度认可。此次检查必将为郑州耐视医药科技有限公司的健康发展奠定良好基础。